Amplatzer™ Talisman PFO Occluder
Amplatzer Talisman PFO オクルーダーは、脳梗塞再発予防のために開発されたPFO閉鎖栓です。
われわれの臨床データは、PFO閉鎖の試験データとして、5810(患者年)の追跡データとなります。
Amplatzer Talisman PFO オクルーダーの導入では、Amplatzer PFO オクルーダーで実証されたテクノロジーをベースに、より多様な症例への対応を目的に30mm-25mmサイズを追加しました。
そして使いやすさの面でも進化をとげています。

公表されている4つの臨床試験では、卵円孔開存(PFO)閉鎖治療が、薬物療法と比較して脳卒中再発のリスクを有意に低減させると報告されています。
その中でもRESPECT試験は長期に患者さんをフォローアップした最大規模の臨床試験であり、PFO閉鎖治療が脳梗塞再発リスクを低減させることが報告されています。
RESPECT試験のハイライト
- 5,810(患者年)の長期追跡データ
- デバイスによるエロージョン、およびデバイス血栓症、脱落の報告ゼロ
- 6か月後の有効閉鎖率は94.2%
- 抗凝固療法を受けている患者さんを組み入れた唯一の臨床試験
RESPECT試験︓PFO閉鎖のターニングポイント
当該試験では、脳梗塞再発予防において、Amplatzer™ PFOオクルーダーによる治療が薬物療法よりも有効であることが示されま した。また、Amplatzer™ PFOオクルーダーによる治療により潜因性脳梗塞の再発リスクを低減することも報告されました。1
References
- Jeffrey L. Saver, et al. N Engl J Med 2017;377:1022-32.
潜因性脳梗塞の再発が相対リスク62%で低減
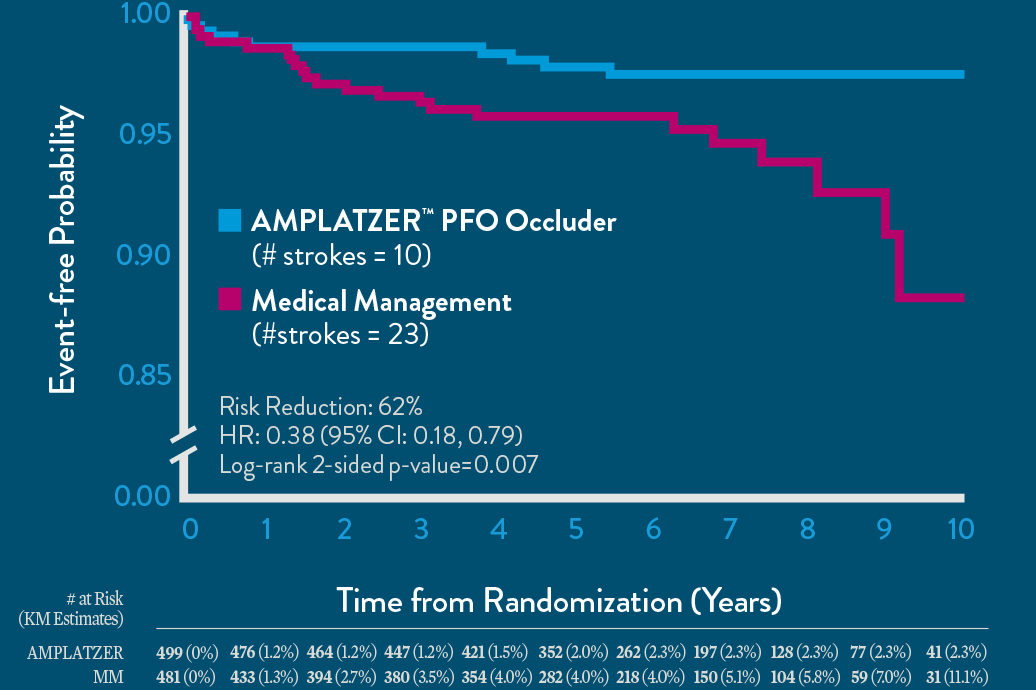
脳梗塞の再発が相対リスク45%で低減
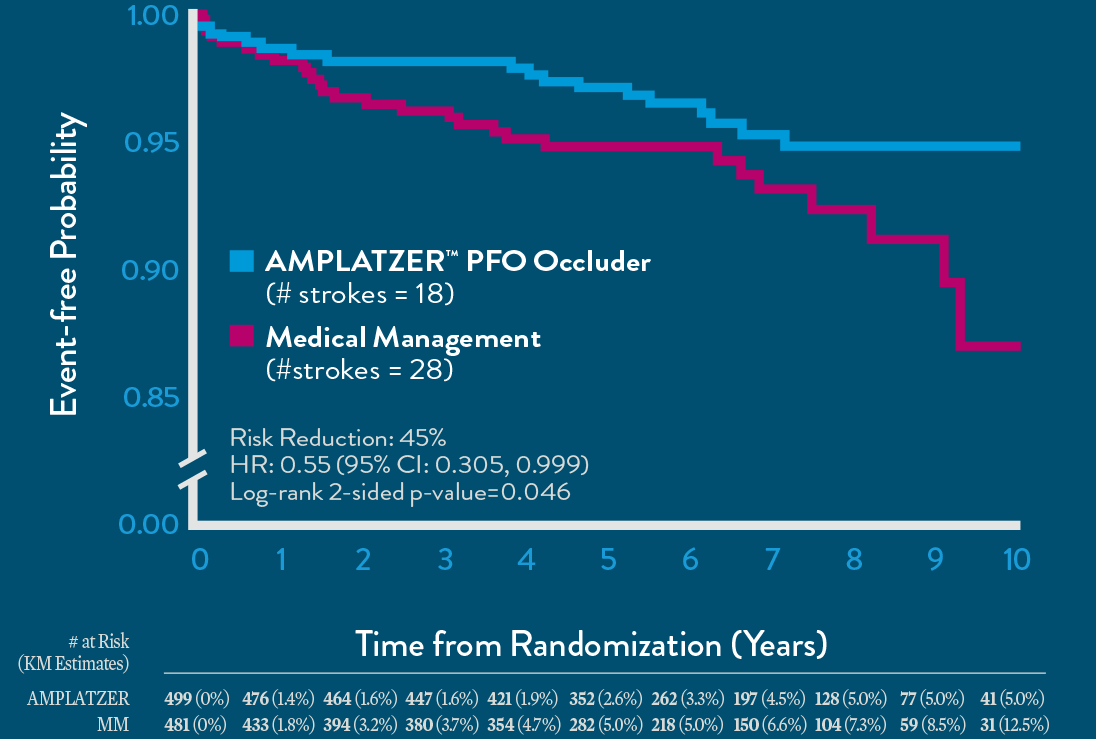
Ordering Information
| SIZING AND DEVICE SELECTION | |||
|---|---|---|---|
| Amplatzer™ Talisman™ PFO Occluder | |||
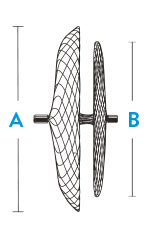
| Model/Reorder Number | Right Atrial Disc Diameter A | Left Atrial Disc Diameter B | Recommended Sheath Size |
| 9-PFO-1818 | 18 mm | 18 mm | 8 F; 45° curve |
| 9-PFO-2518 | 25 mm | 18 mm | 8 F; 45° curve |
| 9-PFO-3025 | 30 mm | 25 mm | 9 F; 45° curve |
| 9-PFO-3525 | 35 mm | 25 mm | 9 F; 45° curve |
| DELIVERY SHEATH | |||||
|---|---|---|---|---|---|
| Amplatzer™ Talisman™ Delivery Sheath | |||||
| Model/Reorder Number | Sheath Size | Tip Angle | Sheath Inner Diameter | Sheath Outer Diameter | Usable Length |
| 9-TDS-08F45-80 | 8 F | 45° | 2.69 mm | 3.45 mm | 80 cm |
| 9-TDS-09F45-80 | 9 F | 45° | 3.00 mm | 3.81 mm | 80 cm |
| 表1 サイズ選択指針 | ||
|---|---|---|
| PFOの形態 | 解剖学的特徴例※ | 推奨サイズ |
| 単純PFO又は顕著でない ASAを伴うPFO 25mmサイズで位置が安定 し、効果的に閉鎖できる PFO |
| 25mm |
| 複合PFO 25mmサイズでは位置が安 定しにくく、 PFOの効果的 な閉鎖を困難にする可能 性がある解剖学的特徴を 伴うPFO |
| 30mm 又は 35mm |
| 小さな形態のPFO 近傍の心腔内組織と干渉 し、25mmサイズが適さな い解剖学的特徴を伴うPFO |
| 18mm |
※心房中隔瘤(ASA):心房中隔の平面から右房又は左房への中隔振幅10mm以上か右房及び左房への総中隔振幅が15mm以上。総中隔振幅が20mm以上を顕著なASAとする。
PFOトンネル長:一次中隔と二次中隔の重なりの最大長。トンネル長10mm以上を長いトンネル長とする。
二次中隔厚さ:PFOから10mm以内の二次中隔の最大厚さ。厚さ10mm以上を二次中隔肥厚、厚さ15mm以上を脂肪腫様過形成を有する二次中隔とする。
【警告】
<使用方法>
- 本品は関係学会の定める「AMPLATZER PFO オクルーダ ーを使用した経皮的卵円孔開存閉鎖術の施設基準」を満 たす施設でのみ使用すること。[適切な施設で使用されな い場合、安全性が担保されないため。]
- 本品は関係学会の定める「AMPLATZER PFO オクルーダ ーを使用した卵円孔開存閉鎖術に関する教育プログラム」 を受けた医師のみが使用すること。[操作上の取扱いに熟 知していない場合には重篤な合併症が発生するおそれが あるため。]
- 脳卒中の知識及び診療経験が豊富な医師と先天性心疾患 もしくは構造的心疾患に対するカテーテルインターベン ションの知識及び診療経験が豊富な医師が協力して本品 の適応を判断すること。[不適切な適応判断により、ベネ フィットが得られない可能性があるため。]
- 静脈血栓塞栓症のリスクが高い患者は卵円孔開存閉鎖術 後、標準治療に続いて血栓塞栓症リスクを低減するレジ メンを用いて管理すること。[血栓塞栓症を引き起こすお それがあるため。]
- 以下のような場合はPFOオクルーダーとデリバリーケー ブルの接続を解除しないこと。 ・PFOオクルーダーの展開不良や、留置後の位置が安定し ない場合 ・留置後PFOオクルーダーが上大静脈(SVC)、肺動脈弁 (PV)、僧帽弁(MV)、冠状静脈洞(CS)、大動脈(AO)等心 腔内組織へ干渉している場合 このような場合はPFOオクルーダーをデリバリーシステム 内に回収し再留置を試みること。それでも不十分であれ ば、新しい製品に交換して留置を試みること。[無理に留 置すると肺動脈塞栓等重篤な合併症が発生するおそれが あるため。]
【禁忌・禁止】
<適用対象(患者)>
- 心臓内に腫瘤、疣贅又は腫瘍が認められる患者、留置予 定部位に血栓を有する患者、卵円孔開存部にアクセスす るための血管に静脈血栓があると診断されている患者。 [血栓塞栓症を引き起こすおそれがあるため。]
- 卵円孔開存部にアクセスするための血管に適切なサイズ のシースを挿入することが困難な患者[本品留置に難渋 し重篤な合併症に至るおそれがあるため。]
- 活動期心内膜炎の患者、または感染症が完治していない 患者。[本品留置に伴い重篤な感染性合併症が起こるおそ れがあるため。]
- 心臓内又は血管内の構造(弁、肺静脈など)により、閉鎖に 必要な本品のサイズが選択できない解剖学的構造の患者。 [PFOオクルーダーが留置部位で安定せず欠損孔から脱落 するおそれがあるため。]
- 右左短絡の原因が他に確認された患者(心房中隔欠損症や 篩状中隔欠損を含む)。[本品のベネフィットが得られな い可能性があるため。]
- 抗血小板療法及び抗凝固療法が実施できない患者。[血栓 塞栓症を引き起こすおそれがあるため。]
- 凝固亢進状態にあることが既知の患者。[血栓塞栓症を引 き起こすおそれがあるため。]
- ニッケルアレルギーのある、又は、その可能性が疑われ る患者。[PFOオクルーダーによってアレルギー反応を引 き起こすおそれがあるため。]
<使用方法>
- 再使用禁止。
- 再滅菌禁止。
販売名::AMPLATZER PFOオクルーダー
承認番号:30100BZX00024000
製造販売元:アボットメディカルジャパン合同会社
MAT-2603547 v1.0
