OCT beseitigt Unklarheiten bei verkalkten Läsionen und ermöglicht so eine ordnungsgemäße Stentexpansion, um optimale Ergebnisse zu erzielen
Kalzium steht mit verringertem Verfahrenserfolg und verringerter Stentexpansion in Verbindung, was zu schlechteren klinischen Ergebnissen führt.1
Häufigkeit und Schweregrad der Koronararterienverkalkung nehmen zu; bis zu 25 % der Patienten bzw. 1 von 4 Patienten weisen eine leichte bis schwere Verkalkung auf.2 Wird die Koronararterienverkalkung nicht diagnostiziert und behandelt, wirkt sich dies negativ auf die PCI-Ergebnisse aus.3
- Kalzifizierte Läsionen begrenzen die Stentexpansion. Dies ist ein wichtiger Prädiktor für das Versagen von Stents, etwa in Form von Stentthrombose und Restenose.1
- Das Erreichen einer optimalen Expansion verringert nachweislich die Rate schwerer kardialer Ereignisse während einer PCI.4
- Eine korrekte Expansion, die durch intravaskuläre Bildgebung bestätigt wird, führt zu einer höheren Sicherheit und Wirksamkeit.4
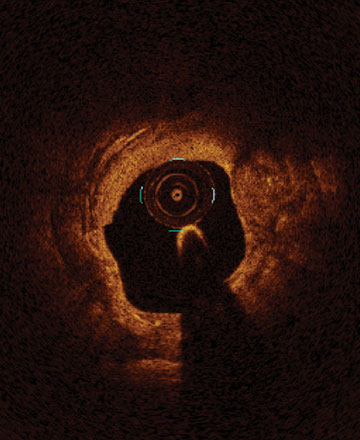
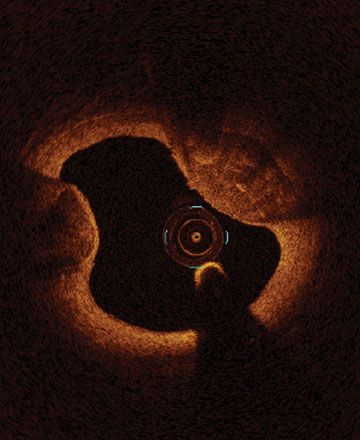
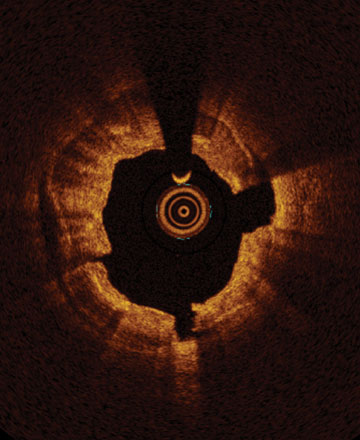
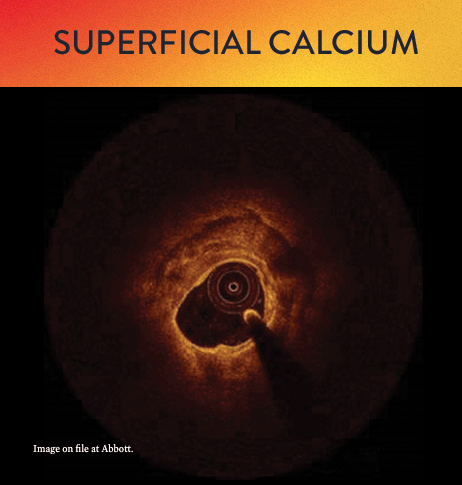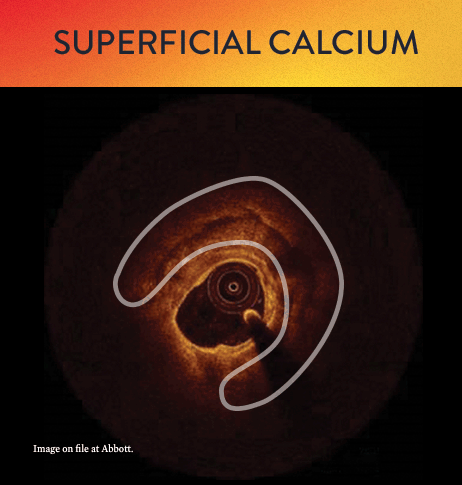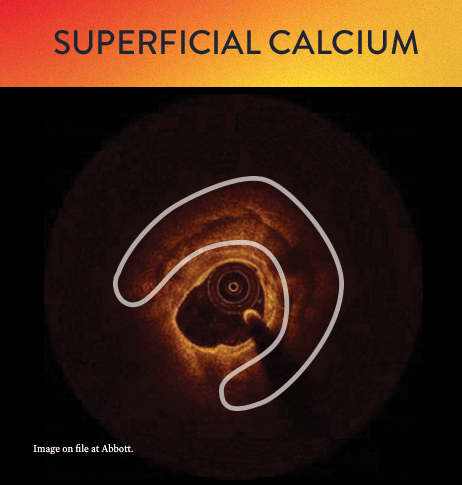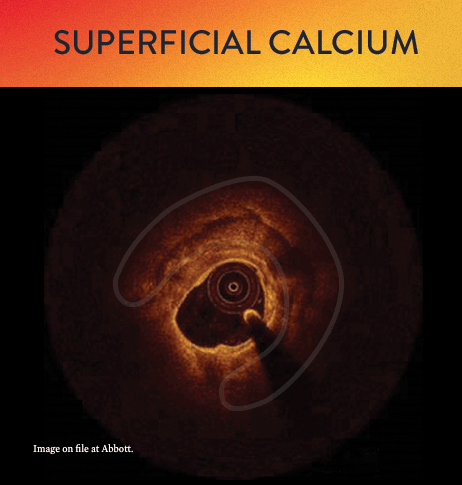
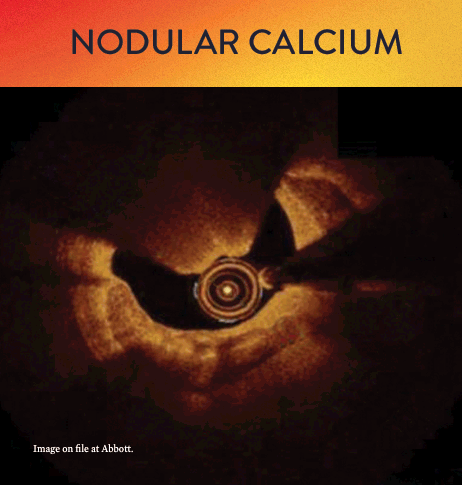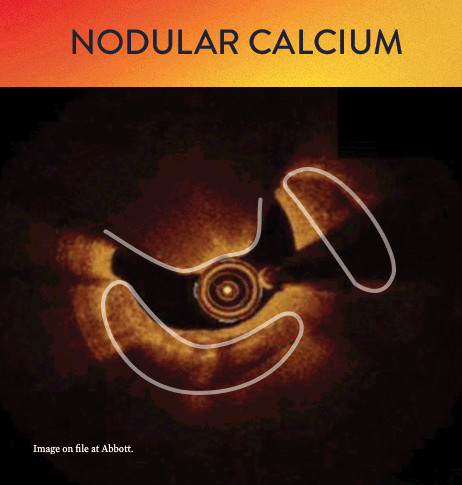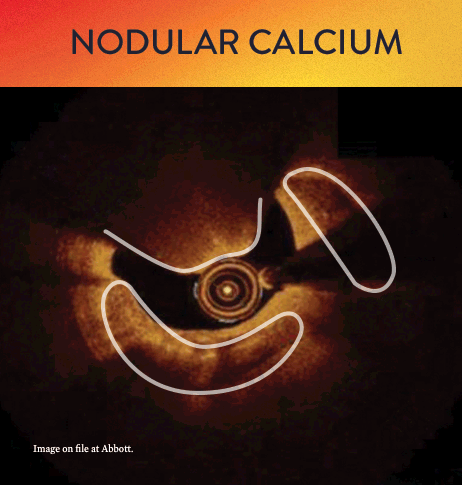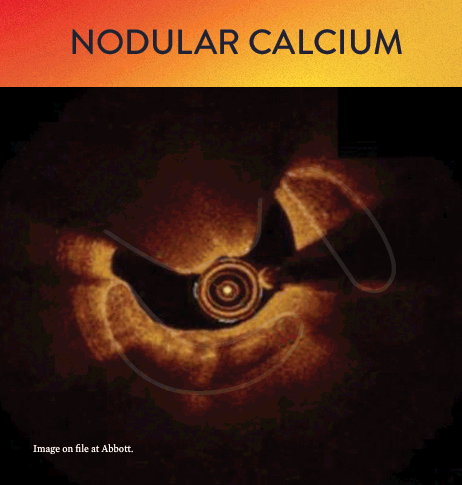
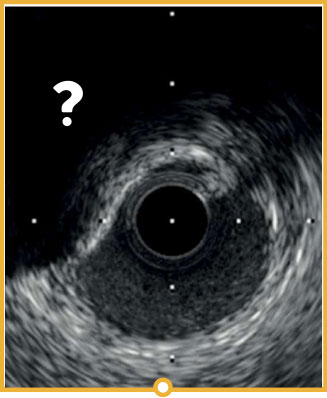
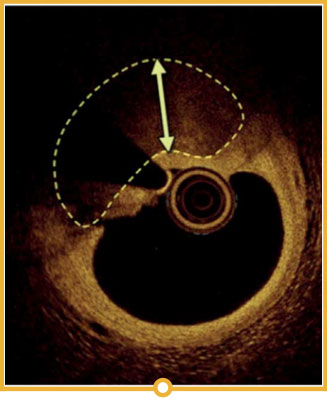
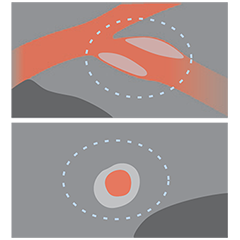
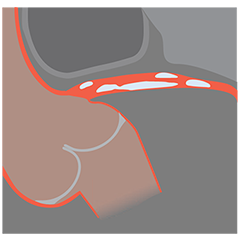
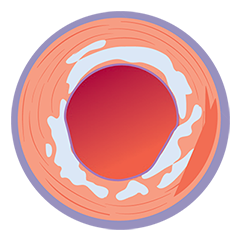
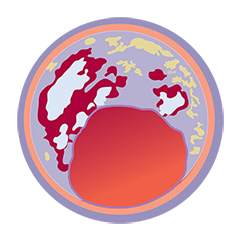
Von links nach rechts: Oberflächliche Kalzifizierung fast 360 Grad; kalzifizierter Knoten von 12-3 Uhr und von 8 bis 10 Uhr; frakturierte oberflächliche konzentrische Kalzifizierung 360 Grad, auf 3-, 6- und 9-Uhr.
Mit der OCT-Bildgebung kann der Grad der Kalzifizierung effektiv charakterisiert und eine optimale Geräteauswahl getroffen werden. Außerdem kann die Wirksamkeit der Behandlung beurteilt werden.1
Der wichtigste Aspekt bei der Bekämpfung von Kalzifizierungsproblemen ist die Erkennung und Klassifizierung von Kalzifizierungen mit der OCT-Bildgebung. Unter Berücksichtigung des Kalzifizierungsgrades können Sie die richtige Strategie zur Läsionsvorbereitung auswählen, die sich auf die Behandlungsstrategie auswirkt.
Der OCT-Workflow, MLD MAX führt den Benutzer Schritt für Schritt durch die Behandlungsentscheidungen vor und nach der PCI. Der erste Schritt des Arbeitsablaufs ist die Beurteilung der Morphologie (M), um zu verstehen, mit welcher Art von Plaque Sie zu tun haben und wie Sie das Gefäß vor dem Stenting am besten vorbereiten. Bei kalzifizierten Läsionen hilft diese Beurteilung, die Art und den Schweregrad der Plaque zu bestimmen.

Im Rahmen der LightLab Clinical Initiative5 haben Ärzte bei fast 1/3 der Läsionen die Strategie zur Läsionsvorbereitung geändert, nachdem sie die Läsionsmorphologie und den Schweregrad mittels OCT beurteilt hatten. In den Fällen, in denen die Strategie zur Gefäßvorbereitung geändert wurde, war Kalzifizierung laut OCT die relevanteste Morphologie.
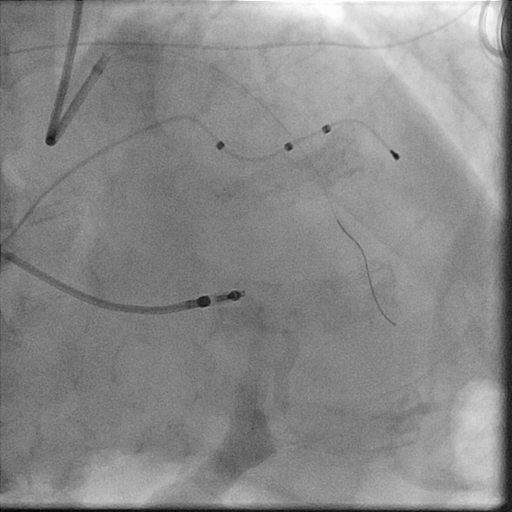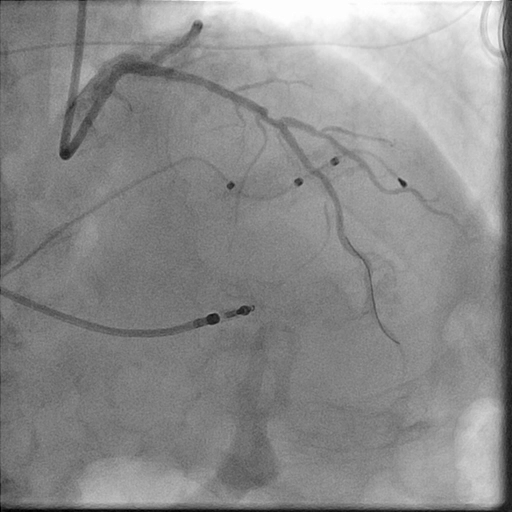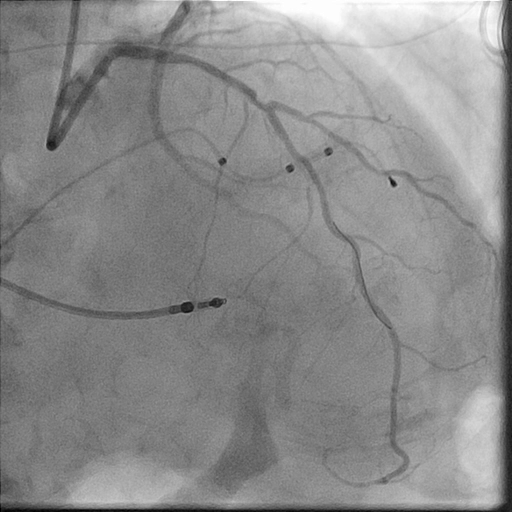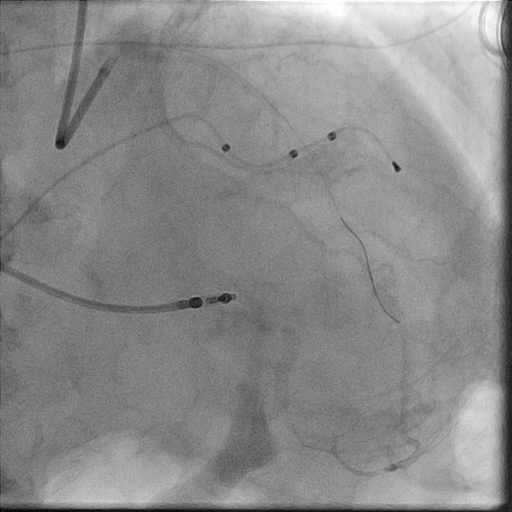
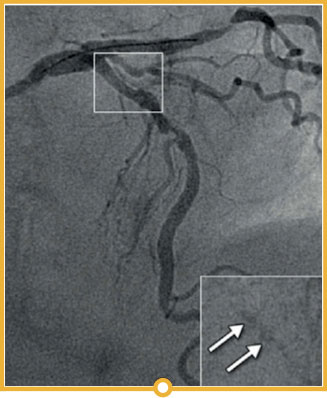
Im LightLab-Fall wurden die Angio-Beurteilung vor der PCI und der geplante Behandlungsansatz (linkes Bild) nach Durchführung der OCT vor der PCI geändert (rechtes Bild).
Änderungen mit den größten Auswirkungen:
- Angiographische Unterschätzung der Kalzifizierung der Läsion (erkannter kalzifizierter Knoten)
- Änderung der Gefäßvorbereitung (von konformem Ballon zu NC-Ballon, Rotationsatherektomie als zusätzliche Maßnahme)
- Änderung der Stentgröße: +6 mm
Morphologie:
Kalzifizierte mittlere LAD-Läsion (Typ B)
hämodynamisch signifikant (IFR = 0,85)
Länge:
30 mm
Durchmesser:
3,0 mm distal, 3,5 mm proximal
Geplante Gefäßvorbereitung: Konforme Ballonbehandlung
geplant: 3,0 mm x 32 mm Stent
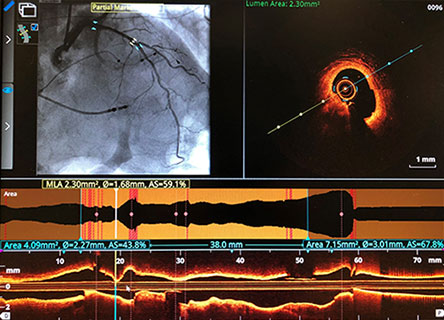
Morphologie:
Kalzifizierte mittlere LAD-Läsion (Typ B)
Länge:
38 mm
Durchmesser:
2,82 mm EEL distal, 3,75 mm EEL proximal
Minimale Lumenfläche: 2,3 mm²
OCT-Gefäßvorbereitung geplant: Nicht konformer Ballon, Rotationsatherektomie
-Behandlung geplant: 3,0 mm x 38 mm Stent
Kalziumklassifizierung gemäß OCT
Die intravaskuläre Bildgebung ermöglicht im Vergleich zur angiographischen Kalziumklassifizierung eine genauere Charakterisierung und Quantifizierung der Kalzifizierung als leicht, mittelschwer oder schwer.
Mit OCT werden Kalzifizierungen als tief, oberflächlich, nodular, exzentrisch oder konzentrisch klassifiziert. Die Morphologie- und Kalziumbeurteilung, die im ersten Schritt des MLD MAX-Arbeitsablaufs, der M-Morphologie, durchgeführt wird, sind wichtige Faktoren zur Bestimmung des optimalen Behandlungsansatzes, da unterschiedliche Kalzium Arten unterschiedliche Behandlungstechniken erfordern.1
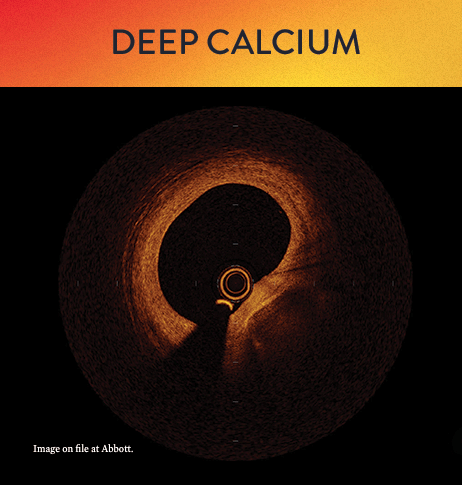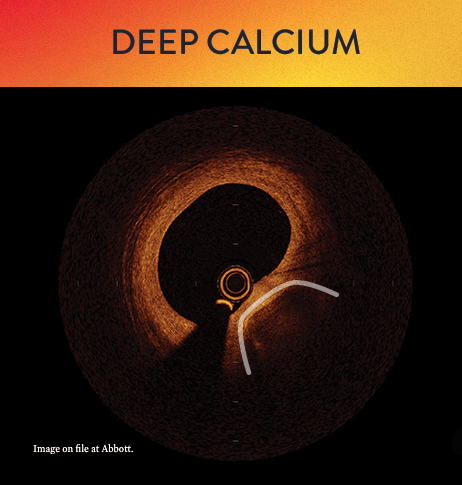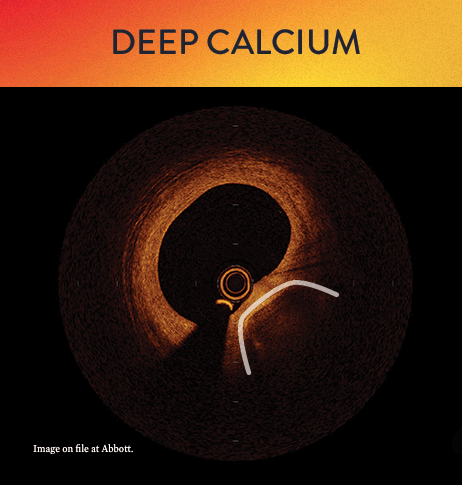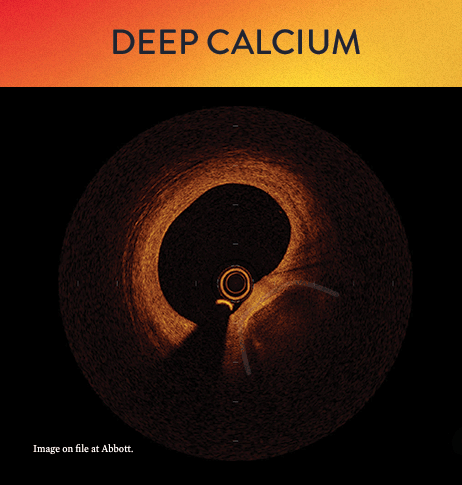
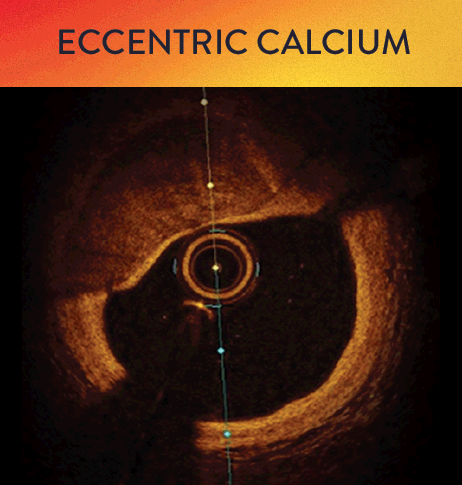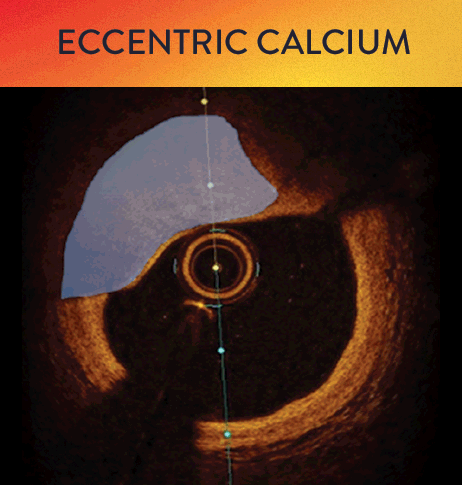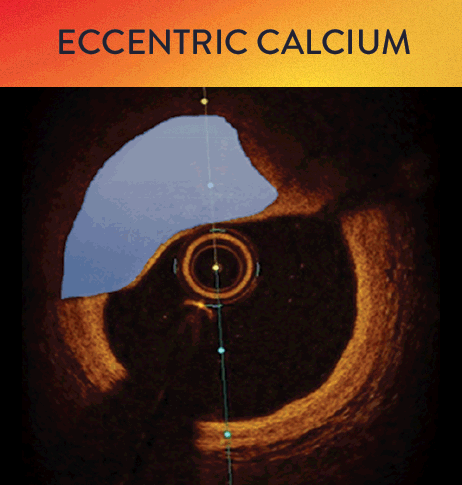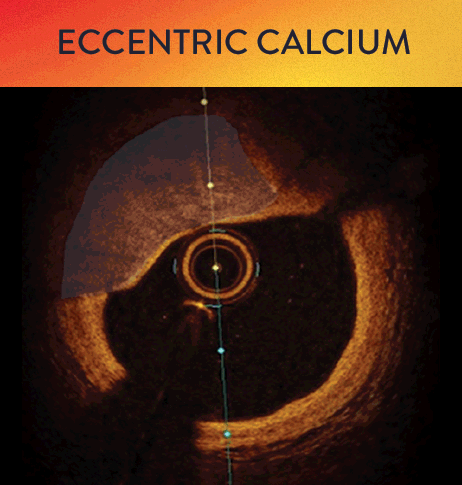

Kalzium-Score bei OCT: 5er-Regel
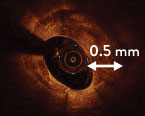
Die Messung der Kalziumtiefe mit einem OCT-basierten Kalzium-Score-Algorithmus kann bei der Erkennung von kalzifizierten Läsionen helfen, bei denen sich eine Plaque-Modifikation vor der Stent-Implantation positiv auswirken würde.6 Dieser Algorithmus untersucht die Dicke, den Winkel und die Länge der Kalzifizierung als wichtigste Parameter zur Prognose des Bedarfs und Nutzens von Geräten zur Kalziummodifikation.
- Dicke > 0,5 mm
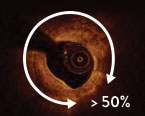
- Winkel > 50 % Gefäßbogen
- Länge >5 mm
Läsionen, bei denen das Risiko einer Stent-Unterexpansion besteht, haben einen Kalzium-Score von 4:6
OCT-BASED CALCIUM VOLUME INDEX SCORE
1Maximum Calcium Angle (°)
≤ 90°
0 point
90° < Angle ≤ 180°
1 point
> 180°
2 points
2Maximum Calcium Thickness (mm)
≤ 0.5 mm
0 point
> 0.5 mm
1 point
3Calcium Length (mm)
≤ 5.0 mm
0 point
> 5.0 mm
1 point
TOTAL SCORE = 0-4 POINTS
5er-Regel
50% vessel arc
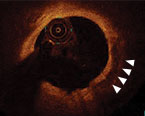
5.0 mm long
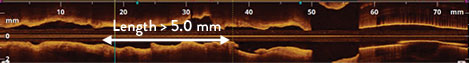
Die Beurteilung der Kalzifizierungsdicke ist entscheidend für die Prognose der Stentexpansion.7 Mit IVUS werden die Schallwellen vom Kalzium reflektiert und erzeugen einen dunklen Schatten. Bei der OCT wird die Kalzifizierungsdicke mittels Durchleuchten festgestellt.7
Diagnose und Behandlung kalzifizierter Läsionen mit OCT
- Starten Sie die PCI mit dem MLD MAX-Workflow
- Beurteilen Sie die Morphologie (M), um den Plaquetyp zu bestimmen
- Wenden Sie bei kalzifizierter Plaque den Algorithmus für die OCT-geführte Behandlung kalzifizierter Läsionen an.1 Der Algorithmus unterstützt die Beurteilung der Kalkablagerung bis zur Läsionsvorbereitung und Behandlung.
Ein solcher Ansatz beruht auf der Möglichkeit, mit OCT Kalkablagerung genau zu erkennen und darauf zuzugreifen, um eine adäquate Gefäßvorbereitung zu ermöglichen (Produktauswahl, Stentgröße) und ausreichende Stentexpansion sicherzustellen.
Video ansehen: OCT-geführte Behandlung von kalzifizierten Läsionen.
In diesem Video erläutert Dr. Tej Sheth die Anwendung des MLD MAX-Algorithmus zur Erkennung und Behandlung verkalkter Läsionen
Wie unterscheidet sich die OCT-Bildgebung von anderen Modalitäten, die bei kalzifizierten Läsionen eingesetzt werden?
OCT ist die beste Bildgebungsmodalität zur Erkennung, Lokalisierung und Quantifizierung von koronaren Kalzifizierungen.8
Die Koronarangiographie, Koronar-Computertomographie (CT), der intravaskulärer Ultraschall (IVUS), die Hochfrequenz (HF), die intravaskulärer Ultraschall-virtuelle Histologie (IVUS-VH) und optische Kohärenztomographie (OCT) können Kalzium lokalisieren und quantifizieren, wenn auch mit sehr unterschiedlicher diagnostischer Genauigkeit. Zu diesem Ergebnis kam Gary Mintz in 20 Jahren intravaskulärer Bildgebungsstudien zum Zusammenhang zwischen Kalzium und koronarer Atherosklerose.8
| Koronarangiographie | CT | IVUS | HF-IVUS (IVUS-VH) | OCT | |
|---|---|---|---|---|---|
| BILDGEBUNGSMODALITÄTEN | 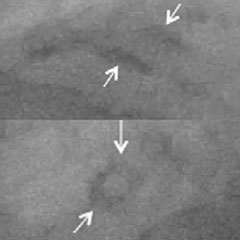 | 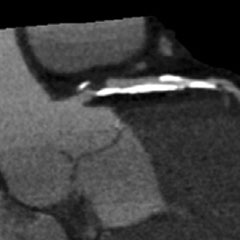 | 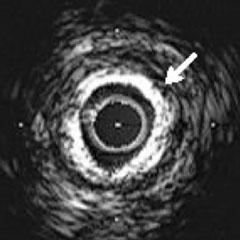 | 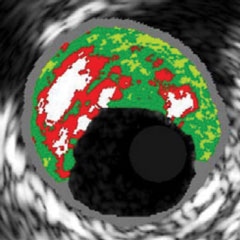 | 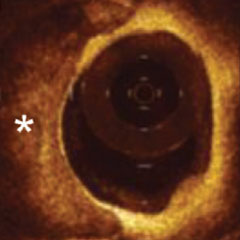 |
| Erkennung von Kalzium in den Koronararterien | + | +++ | +++ | +++ | ++++ |
| Lokalisierung von Kalzium in den Koronararterien | + | +++ | +++ | +++ | ++++ |
| Quantifizierung des Kalziums in den Koronararterien | + | +++ | ++ | +++ | ++++ |
 |  |  |  |  |
Der Erfolg der PCI und die Reduzierung zukünftiger Revaskularisationen hängen stark von der finalen Stentexpansion ab.1 Die Koronararterienverkalkung wird bei der Angiographie häufig unterschätzt, da die Angiographie den Schweregrad der morphologischen Läsion unterschätzt, was wiederum Auswirkungen auf die Behandlungsstrategie hat.5
Die Verwendung der OCT-Bildgebung und des MLD MAX-Workflow als Orientierungshilfe für die PCI hilft bei der Bestimmung des richtigen Behandlungsansatzes und der optimalen Stentexpansion. Bei LightLab erzielten Operatoren bei Anwendung des MLD MAX-Workflows durchschnittlich eine Stentexpansion von mindestens 80 %.
Literaturhinweise
- Shlofmitz, E., Sosa, F. A., Ali, Z. A., Waksman, R., Jeremias, A., & Shlofmitz, R. (2019). OCT-Guided Treatment of Calcified Coronary Artery Disease: Breaking the Barrier to Stent Expansion. Current Cardiovascular Imaging Reports, 12(8), 32.
- Dean Kereiakes, Disrupt CAD III: Lithotripsy for Vessel Preparation in Calcified Coronary Arteries Prior to Stenting, CLD. Dec 29, 2020.
- Madhavan MV, Tarigopula M, Mintz GS, Maehara A, Stone GW, Généreux P. Coronary artery calcification: pathogenesis and prognostic implications. J Am Coll Cardiol. 2014 May 06;63(17):1703-14.
- Räber L, et al. Clinical use of intracoronary imaging. Part 1: guidance and optimization of coronary interventions. An expert consensus document of the European Association of Percutaneous Cardiovascular Interventions. Eur Heart J. 2018;39(35):3281-3300.
- Croce, K. et al: Optical Coherence Tomography Influences Procedure and Vessel Preparation Decisions During Percutaneous Coronary Intervention– Insights from the LightLab Initiative. TCTConnect2020 Presentation.
- Fujino, A et al. A new optical coherence tomography-based calcium scoring system to predict stent underexpansion. EuroIntervention. 2018 Apr 6;13(18):e2182-e2189. doi: 10.4244/EIJ-D-17-00962.
- Wang, X et al. In vivo calcium detection by comparing optical coherence tomography, intravascular ultrasound, and angiography. JACC Cardiovasc Imaging. 2017 Aug;10(8):869-879. doi: 10.1016/j.jcmg.2017.05.014.
- Mintz,G. Intravascular Imaging of Coronary Calcification and its Clinical Implications. JACC Cardiovascular Imaging, 2015. http://dx.doi.org/10.1016/j.jcmg.2015.02.003
MAT-2112906 v1.0

