Orbital Atherectomyは、高度石灰化を伴う複雑なPCI症例における至適なプレパレーションのための最初の一手です。
冠動脈石灰化は過小評価される傾向があります。血管造影で軽度または中等度と考えられる石灰化は、血管内超音波検査(IVUS)や光干渉断層撮影(OCT)などの高度な画像検査を使用すると、実際には重度であることが判明することがあります。1,2 PCIを受ける患者の30〜40%が中等度から重度の石灰化病変を、有します。2,3
石灰化による難航事象4
- バルーン血管形成術または前拡張中に解離しやすい
- バルーンを十分に拡張することが難しい
- ステントのデリバリーが妨げられる
- 至適なステントの拡張と留置が妨げられる
Diamondback 360™ OASは、2,200人以上の患者を対象とした11の臨床研究で、高度石灰化病変の治療に対する有効性と安全性が報告されています。5,6
ORBIT II 臨床試験7
ORBIT IIピボタル試験は、米国で実施された前向き多施設共同研究で、ステント留置前にDiamondback 360™ Coronary Orbital Atherectomy システム (OAS) Classic Crownで治療された冠動脈高度石灰化病変の患者を評価しました。
主なポイント
- ORBIT IIは、安全性と有効性のプライマリーエンドポイントを達成した7
- ORBIT IIは、薬剤溶出性ステントサブセット(N = 389/443)で、1年で3.4%、3年で6.6%という低い標的病変血行再建術(TLR)率を示した8
スタディデザイン7
- 高度石灰化病変を有する443人の患者が、米国の49の施設で登録
- Diamondback 360™ Coronary OASClasic Crownの安全性と有効性を評価する
- 安全性のプライマリーエンドポイント:30日時点の主要な心血管有害事象(MACE)
- 有効性のプライマリーエンドポイント: ステント残存狭窄率50%未満でかつ院内MACE発生がないことを手技の成功の定義とする
PATIENT POPULATION7
| N=443 | |
|---|---|
| History of Diabetes | 36.1% |
| History of CABG | 14.7% |
| History of Dyslipidemia | 91.9% |
| History of Hypertension | 91.6% |
| Smoker (current or previous) | 66.1% |
STUDY RESULT7
| Procedural Success | 88.9% |
|---|---|
| Successful Stent Delivery | 97.7% |
| Less than 50% Residual Stenosis | 98.6% |
| Freedom from in-hospital MACE | 90.2% |
*Procedural success defined as success in facilitating stent delivery with a residual stenosis of <50% and without the occurrence of an. in-hospital MACE.
30-Day Outcomes9
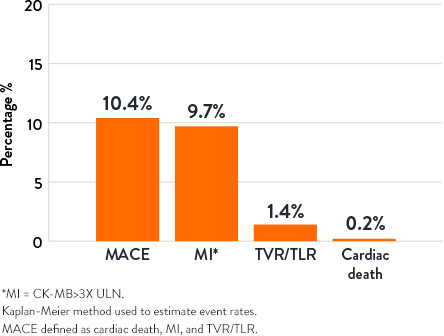
1-Year Outcomes9
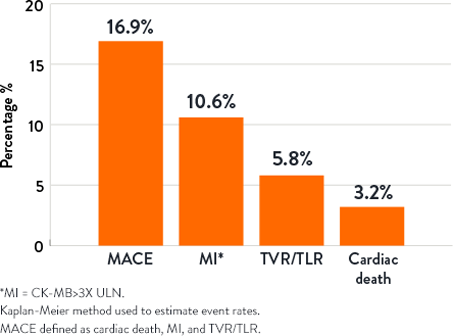
本WEBページ上のイラスト/製品画像は全てイメージ図です。実際の縮尺とは違いがあります。
販売名:Diamondback 360 Coronary Orbital Atherectomy システム 医療機器承認番号:22900BZI00004000 分類:高度管理医療機器
選任製造販売業者: アボットメディカルジャパン合同会社
外国特例承認取得者: Cardiovascular Systems, Inc.
カーディオバスキュラー システムズ インク(米国)
References
- Mintz GS. Intravascular imaging of coronary calcification and its clinical implications. JACC Cardiovasc Imaging. 2015;8(4):461-471.
- Mintz GS, et al. Patterns of calcification in coronary artery disease. A statistical analysis of intravascular ultrasound and coronary angiography in 1155 lesions. Circulation. 1995;91(7):1959-1965.
- Genereux P, et al. Ischemic outcomes after coronary intervention of calcified vessels in acute coronary syndromes. Pooled analysis from the HORIZONS-AMI (Harmonizing Outcomes With Revascularization and Stents in Acute Myocardial Infarction) and ACUITY (Acute Catheterization and Urgent Intervention Triage Strategy) TRIALS. J Am Coll Cardiol. 2014;63(18):1845-1854.
- Shlofmitz E, et al. Orbital atherectomy for the treatment of severely calcified coronary lesions: evidence, technique, and best practices. Expert Rev Med Devices. 2017;14(11):867-879.
- Shlofmitz, E., et al., Lesion Preparation with Orbital Atherectomy. Interv Cardiol. 2019;14(3):169-173. .
- Beohar, N., Orbital Atherectomy for Treating De Novo Severely Calcified Coronary Lesions. A Tertiary Center Experience, Presented at TCT Connect 2020.
- Chambers JW, et al. Pivotal trial to evaluate the safety and efficacy of the orbital atherectomy system in treating de novo, severely calcified coronary lesions (ORBIT II). JACC Cardiovasc Interv. 2014;7(5):510-518.
- Data on file at Abbott.
- Lee M, et al. Orbital atherectomy for treating de novo, severely calcified coronary lesions: 3-year results of the pivotal ORBIT II trial. Cardiovasc Revasc Med. 2017;18(4):261-264.
MAT-2408357 v2.0
