Supera™ Periphere Stents
Der periphere Supera™ Stent ist eine einzigartige Stentklasse für Behandlungen in der A. femoralis superficialis (AFS). Dieser Stent ist aus ineinander verwobenen Nitinoldrähten gefertigt und bietet den Ärzten unübertroffene klinische Ergebnisse1-12 bei Läsionen unterschiedlichster Komplexität und Länge.1, 13-15
Die Ergebnisse zählen
Der periphere Supera™ Stent wurde bereits bei mehr als 2.000 Patienten und in 17 Studien weltweit untersucht1,15-30 und ist für seine hervorragenden klinischen Ergebnisse nach perkutanen transluminalen Angioplastien (PTA) mit Stentplatzierung bekannt.
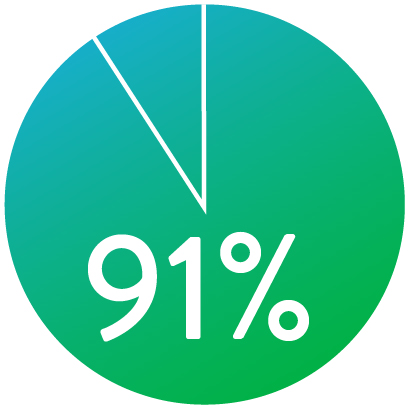
OFFENHEIT (K-M) NACH 1 JAHR
Bei nominaler Freisetzung *
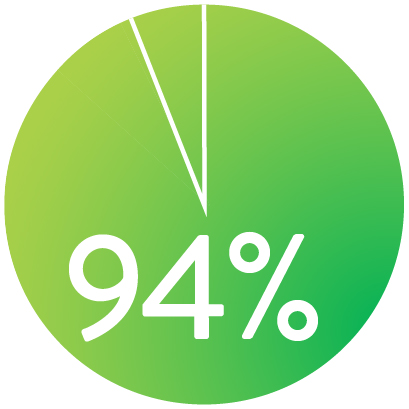
FREIHEIT VON
REVASKULARISATION DER
ZIELLÄSION (TLR) NACH 3 JAHREN
Bei nominaler Freisetzung *
*Nominale Freisetzung ist definiert als Freisetzung in einem Bereich von +/- 10 % der angegebenen Stentlänge. Diese Daten stammen aus einer nicht-gepowerten Post-hoc-Analyse.
Zeigt hervorragende klinische Ergebnisse
Der Supera™ Stent zeigte in der SUPERB-Studie exzellente Offenheit nach 1 Jahr und die Freiheit von TLR nach 3 Jahren.1
1
Unübertroffene klinische Ergebnisse
Zeigt unübertroffene klinische Ergebnisse bei einfachen Läsionen1-12
2
Konsistente Offenheit unabhängig von der Läsionslänge *
Konsistente Ergebnisse der primären Offenheit nach 1 Jahr unabhängig von der Läsionslänge13-20,31
3
Gute Ergebnisse in kalzifizierten Läsionen
Zeigt nach 3 Jahren gute klinische Ergebnisse bei stark kalzifizierten Läsionen1
In die Studie eingeschlossen wurden 93,8 % Läsionen von Typ A und B nach der Trans-Atlantic InterSociety Consensus-Klassifikation (TASC) und/oder Läsionen der Klasse 2 oder 3 Läsionen nach Rutherford.
* Die Offenheitsraten wurden in Studien mit Läsionslängen von 5,3 cm bis 28,0 cm evaluiert.
Die Plattform zählt
Im Gegensatz zu anderen Stentplattformen ist der Supera™ Stent durch seine besondere Konstruktion aus einzelnen, ineinander verwobenen flexiblen Nitinoldrähten in einzigartiger Weise in der Lage, Gefäße offen zu halten.
Hoher Kompressionswiderstand32
4x höherer Kompressionswiderstand – so dass ein rundes, offenes Gefäßlumen erhalten bleibt, was besonders bei kalzifizierten Läsionen von Vorteil sein kann
Geringe chronische Aufstellkraft (Chronic Outward Force)32
Bei einer Größe von 1:1 von Stent zu Gefäß führt eine geringe chronische Aufstellkraft zu einer minimalen Gefäßverletzung.34
Hohe Flexibilität33 und Bruchfestigkeit1
Unübertroffene Flexibilität,33 die die natürliche Struktur und Bewegung der Gefäßanatomie nachahmt35-37
Bei mehr als 2.000 Patienten wurden nach einem Jahr in 17 Studien keine Stentfrakturen nachgewiesen1,15-30
LITERATURHINWEISE
- Garcia L. et al., Catheterization and Cardiovascular Interventions 2017 Jun 1;89(7):1259-1267.
- Dake M. et al., Circulation. 2016;133:1472-1483.
- Laird J. et al., Circ Cardiovasc Interv. 2010;3:267-276.
- Laird J et al., J Endovasc Ther. 2012;19:1-9.
- S.M.A.R.T. Control IFU.
- Jaff, M., SMART Nitinol Self-Expanding Stent in the Treatment of Obstructive Superficial Femoral Artery Disease: Three-year Clinical Outcomes from the STROLL Trial. ISET 2014.
- Matsumura J et al., J Vasc Surg 2013;58:73-83.
- Rocha-Singh, K., 3-Year Results of the DURABILITY II Study. VIVA 2013.
- US Innova IFU.
- US Pulsar IFU.
- Ohki T. et al. J Vasc Surg. 2016 Feb;63(2):370-6.
- Gray W. et al., Lancet 2018;392:1541-51.
- Treitl, K.M., et al. European Radiology.2017; 10.1007.
- Palena L.M. et al. Catheterization and Cardiovascular Intervention.2016.
- Brescia AA. et al., J Vasc Surg. 2015 Jun;61(6):1472-8
- George JC. et al., J Vasc Interv Radiol. 2014 Jun;25(6):954-61.
- Montero-Baker M. et al., J Vasc Surg. 2016 Oct;64(4):1002-8.
- Scheinert D. et al., J Endovasc Ther. 2011 Dec;18(6):745-52.
- Werner M. et al., EuroIntervention. 2014 Nov;10(7):861-8.
- San Norberto EM. et al., Ann Vasc Surg. 2017 May;41:186-195.
- Chan YC. et al., J Vasc Surg. 2015 Nov;62(5):1201-9.
- Dumantepe M. Vasc Endovascular Surg. 2017 Jul;51(5):240-246.
- Goltz JP. et al., J Endovasc Ther. 2012 Jun;19(3):450-6.
- León LR Jr. et al., J Vasc Surg. 2013 Apr;57(4):1014-22.
- Myint M. et al., J Endovasc Ther. 2016 Jun;23(3):433-41.
- Palena LM. et al., J Endovasc Ther. 2018 Oct;25(5):588-591.
- Scheinert D. et al., JACC Cardiovasc Interv. 2013 Jan;6(1):65-71.
- Steiner S. et al., J Endovasc Ther. 2016 Apr;23(2):347-55.
- Teymen B. et al., Vascular. 2018 Feb;26(1):54-61.
- Bhatt H. et al., Cardiovasc Revasc Med. 2018 Jul;19(5 Pt A):512-515.
- Garcia L. et al. Circ Cardiovasc Interv. 2015;8:e000937
- Zu den getesteten Konkurrenzprodukten gehören Astron Pulsar-18, Complete SE, EverFlex, Innova, LifeStent, Misago, S.M.A.R.T. und Zilver PTX. Tests durchgeführt von und Daten verfügbar bei Abbott.
- Flexibilität ist definiert als Knickfestigkeit. Zu den getesteten Konkurrenzprodukten gehören Astron Pulsar-18, Complete SE, EverFlex, Innova, LifeStent, Misago, S.M.A.R.T. und Zilver PTX. Tests durchgeführt von und Daten verfügbar bei Abbott.
- Zhao HQ et al. Cardiovasc Intervent Radiol. 2009;32(4):720-6
- Arena F. et al., J Vasc Med Surg. 2013:1;116.
- Chen Y. et al., J Vasc Surg 2014;59:384-91.
- Tests durchgeführt von und Daten verfügbar bei Abbott.
MAT-2114731 v1.0
